-
电话:19390038897
-
微信:2777177595
-
QQ:2777177543QQ:2777177543
-
邮箱:2777177543@qq.com

真核细胞膜系统形成具有特定形态、特化功能的多种膜性细胞器。膜性细胞器之间的精细分工与相互协作使得它们在结构和功能上形成有序的网络,这既能维持细胞器的稳态,又可以实现有效的物质信息交流。细胞器形态的破坏以及细胞器互作网络的紊乱与多种疾病发生发展密切相关。因此,细胞的正常生命活动需要膜性细胞器的稳定形态和有序的细胞器互作网络。然而,细胞器之间有序互作的方式、功能和机制仍未阐明。
鉴于结构对功能的决定性作用,中国科学院长春应用化学研究所王宏达研究员,课题组创新提出从膜系统整体结构的角度来研究细胞器的有序互作机制。在前期工作中,该团队利用多种单分子技术对细胞膜整体结构和膜蛋白分布特征进行了系统性研究,发现细胞膜结构具有膜蛋白非对称性分布的特征,并原创提出了血红细胞“半镶嵌”结构模型和哺乳动物组织细胞“蛋白层-磷脂-蛋白岛”结构模型。近期,经过仔细分析细胞膜、转运囊泡膜、高尔基体膜结构后,发现它们具有相反或相同的膜蛋白非对称性;因此该团队推测膜的结构特征可能决定了细胞器的有序互作方式。
为了验证这一假设,该研究团队以生长因子受体蛋白的囊泡运输过程为研究对象,在对膜结构特征进行静态分析基础上,通过实时示踪方法追踪囊泡运输与融合全过程。研究发现内吞囊泡外膜的蛋白突起阻碍它们彼此进一步接触,因而囊泡进行有序的运输而非随机融合;同时内吞囊泡粗糙外膜暴露的磷脂决定了它们之间在特异性融合蛋白的介导下能够通过磷脂的互相插入而发生完全的膜融合;高尔基体外膜致密的蛋白层致使内吞囊泡只能通过kiss-on-run(接触后即离开)的方式与其进行交流。通过以上研究,该团队首次提出了一种新的囊泡有序转运的模型“膜不对称性决定有序的细胞器转运”,即Membrane-asymmetry-determined orderly organelle transport (MADOOT),它为细胞内错综复杂的有序转运事件提供了合理解释。
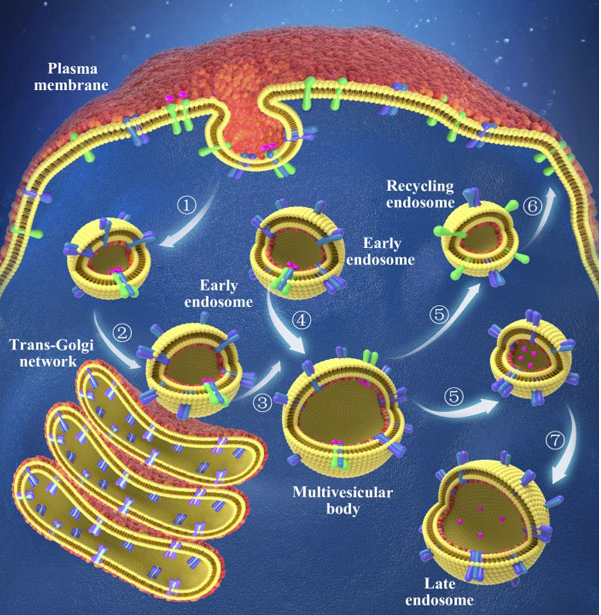
图1. 受体蛋白内吞与循环过程中囊泡有序运输的结构机制示意图。①内吞囊泡的形成。膜蛋白在细胞膜和内吞囊泡膜上具有相反的非对称性。②受体蛋白被运输到早期内含体。③早期内含体囊泡与高尔基体反面囊膜接触后即离开。④同型早期内含体囊泡发生完全膜融合后形成多泡体。⑤内含体发生分剪导致受体蛋白与配体分开。⑥受体蛋白通过循环内含体返回细胞膜。⑦配体被分选到晚期内含体。
